以盆栽黄连花( Lysimachia davurica)幼苗为材料,研究了20 d的干旱胁迫和复水对植株部分形态特征及叶片抗旱相关生理指标的影响。结果表明,随着胁迫时间的增加,其生长发育逐渐受到抑制。当胁迫时间低于10 d以及土壤含水量不低于14.52%时,其地上部生长受到一定的抑制,叶片失水,单叶面积减小,叶绿素含量、MDA含量、可溶性糖、脯氨酸以及抗氧化酶(POD、CAT)活性升高,此时复水,除了茎尖,植株可以迅速恢复生长。当胁迫时间持续增加到15 d,叶片严重失水,地上部干枯,此时复水,66.66%的植株可以重新长出幼苗。但当胁迫时间达到20 d时,植株因缺水干旱死亡。因此,黄连花在管理养护时,在持续干旱时间超过10 d,土壤含水量低于14.52%时,应及时复水救苗。
The effect of 20 d drought stress and rewatering on seedling morphological and physiological characteristics of Lysimachia davurica were studied. The results showed that growth and development of L. davurica were gradually inhibited as drought stress extended. The growth of above ground part of seedling was depressed first when drought stress lasted for less than 10 days and soil moisture content was higher than 14.52%. The leaf area and relative water content were reduced, while chlorophyll content, MDA content, soluble sugar, proline, POD and CAT activities of seedling were increased. The plant could quickly restored growth except the shoot tip when rewatering at this time. When drought stress lasted for 15 days, the seedling severely lost water and the upper part of the seedlings shriveled. 66.66% new sprout grew after rewatering. L. davurica would be dying and could not be revived after rewatering if drought stress lasted for 20 days. Therefore, L. davurica should be rewatered timely to rescue seedling when the drought stress was more than 10 days and the soil moisture content was less than 14.52%.
干旱从古至今都是人类面临的主要自然灾害[1], 也是制约植物正常生长的关键因素[2], 因而合理有效的利用水资源成了全球关注的问题。研究表明, 植株在逆境下会通过保护酶活性的变化对不良环境做出响应。轻度的干旱胁迫对植株的影响较小, 复水后, 植株的形态、生理特征等均可缓慢恢复, 是一个可逆的过程。这样既可以保证植株的正常生长, 又可以节水, 使紧张的水资源得到有效合理的利用, 这成为了当今的研究热点。
黄连花(Lysimachia davurica)是报春花科珍珠菜属(Lysimachia)的多年生草本植物, 在国内主要分布于黑龙江、吉林、辽宁、内蒙、北京、山西、陕西和云南等地, 其花期在春末至秋初, 花期长, 花大、色黄、密集, 具有很高的观赏价值, 且其耐寒性强, 在寒冷的东北地区根部宿存于地下而不死, 是较为理想的高寒地区绿化资源。同时黄连花还是一种重要的药用材料, 具有镇静、降压、治失眠和高血压的功效[3]。目前, 关于珍珠菜属过路黄(L. christinae)的高温胁迫[4]、低温胁迫[5, 6, 7]、干旱胁迫[8]、盐胁迫[9, 10]及光适应性[11]方面等研究报道较多。而关于黄连花的研究主要集中在其化学成分的鉴定、分离提取[12, 13, 14]、种子萌发、组培体系的建立[15, 16]以及其驯化栽培[17]等方面, 尚未见到干旱胁迫及复水对黄连花幼苗生长影响的报道。本研究以黄连花幼苗为试验材料, 通过研究干旱胁迫及复水对黄连花部分形态指标及叶片抗旱相关生理指标的影响, 探索其可以承受土壤干旱的程度, 从而为其抗性机制的研究奠定基础, 同时可以在生产上掌握其临界点, 从而进行科学的水分管理并避免伤害。
试验于东北林业大学园林学院花圃的温室进行。黄连花的组培苗经过缓苗、驯化、移栽后作为备用试验材料。2015年4月选择高度约为8 cm, 生长状况基本一致的黄连花生根苗, 移栽到装有蛭石的花盆中进行驯化20 d。其间每周浇灌一次稀释了5~10倍的MS营养液10 mL为其补充营养。驯化结束后, 将黄连花移栽至花盆中(上口径13 cm, 下口径9.5 cm, 高11 cm), 每盆装花卉市场上购买的育苗基质土300 g进行正常的栽培管理, 育苗基质土壤pH 4.59, 有机质含量15.27 g· kg-1, 全N含量18.52 g· kg-1, 全P含量3.3 g· kg-1, 全K含量21.41 g· kg-1。
2015年6月14日进行黄连花的自然干旱胁迫(此时植株的高度为21.55 cm)。温室的温度变化范围为 28-38 ℃。试验设置了4个干旱梯度:胁迫时间分别为5、10、15和20 d, 每个梯度6盆。试验前1 d充足浇水, 使土壤水分达到饱和, 作为干旱开始(0 d)。开始控水后, 对照组每天09:00对其进行补水, 使其土壤含水量[18]控制在85%~87%。在胁迫5、10、15和20 d时对株高和土壤含水量进行测量, 并分别剪取叶片, 将其包于锡箔纸中, 立即带回实验室, 并储藏于-80 ℃冰箱中, 用于测定叶片含水量、单叶面积、叶绿素含量、脯氨酸含量、丙二醛等生理指标。胁迫5、10、15 d、取样后即刻复水(以花盆底部有水流出为准), 复水后5 d, 取恢复生长的叶片, 分别测定其各项生理指标, 15 d后统计其成活率。
黄连花的株高采用卷尺测量基部到植株最高部位的自然距离; 叶片相对含水量采用烘干称量法测定[19]; 土壤含水量采用烘干法测定[18]; 单叶面积的测定采用透明方格网法[18]; 叶绿素含量采用95%的乙醇提取法[20]; 脯氨酸含量的测定采用酸性茚三酮法[21]; 叶片SOD活性采用氮蓝四唑(NBT)光还原法[21]; POD活性采用愈创木酚法[21]; CAT活性采用紫外分光光度法[21](UV/VIS sprectrometer型号紫外可见分光光度计测定吸光值); 叶片丙二醛(MDA)含量和可溶性糖含量采用硫代巴比妥酸法[21]; 成活率以胁迫后复水原植株保持生命力或萌发新芽为标准。
采用Excel 2003对所有数据进行初步整理和作图, SPSS 19.0进行One-way ANOVA单因素方差和显著性分析。
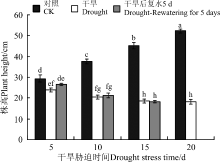
当幼苗遭受干旱胁迫时, 随着土壤含水量的减少, 幼苗的平均高度呈下降趋势, 且显著低于对照(P< 0.05)(图1)。0-15 d干旱胁迫下, 株高降幅较明显, 15-20 d变化不明显。恢复供水5 d后, 干旱5 d的株高有所增加, 但仍低于对照, 干旱10和15 d复水前后的变化不显著(P> 0.05)。
干旱5 d时, 黄连花叶片出现轻度萎蔫现象, 与茎尖方向的夹角变大。复水后, 植株恢复正常。当胁迫达到10 d时, 叶片皱缩严重, 萎蔫下垂, 特别是茎尖严重缺水, 以致弯曲下垂。复水后, 植株下部叶片的外部形态基本恢复正常, 茎尖依然萎蔫枯黄, 接近茎尖的叶片叶尖枯黄, 但是腋芽开始萌发, 这可能与顶端优势破坏有关。胁迫15 d时, 地上部分干枯, 此时复水, 可以重新长出幼苗。但到20 d时, 植株干旱死亡。
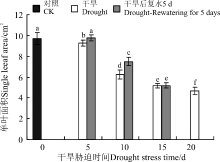
生长在干旱环境中的植物, 叶片在结构上主要向着降低蒸腾、增强储水性和提高光合方面发展[22]。其中, 叶面积减小被认为是幼苗对于干旱胁迫的反应之一[23]。随着干旱胁迫程度的加剧, 黄连花的单叶面积呈现逐渐下降的趋势, 且在5-10 d时, 降幅较大(图2)。恢复供水5 d后, 胁迫5和10 d的单叶面积均有不同程度的恢复, 而干旱15 d复水后, 单叶面积的变化不显著。这表明短时间的干旱胁迫对黄连花的影响不明显, 但是胁迫时间过长就会影响叶片的光合等特性。
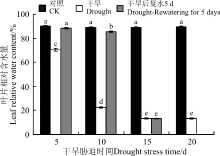
RWC是干旱条件下细胞脱水的一个重要指标[24]。干旱胁迫下, 黄连花叶片相对含水量逐渐降低, 在胁迫的各个时间点均显著低于对照(P< 0.05)。在胁迫5、10、15和20 d时分别较对照下降了21.07%、74.83%、84.22%和85.05%。5 d的干旱胁迫对RWC的影响显著, 而且随着胁迫时间的延长, RWC显著下降, 尤其是在胁迫时间为5-10 d时, RWC下降更为明显, 当胁迫超过10 d时, 变化较为缓慢(图3)。复水5 d后, 干旱5 d和10 d的叶片RWC迅速回升, 而干旱15 d的RWC却无明显变化, 说明黄连花在短期的胁迫下复水可以迅速恢复, 而在长期的胁迫条件下, 由于植株受到了严重的伤害, 短时间内无法恢复。
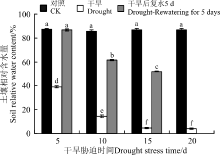
干旱胁迫是栽培土壤缺乏对植物有效的水分供给, 从而影响植物正常的生长。随着干旱胁迫时间的延长, 土壤含水量呈现逐渐下降的趋势, 胁迫时间越长, 影响越严重(图4)。0-15 d时, 土壤含水量急剧下降, 15-20 d时变化不明显。胁迫5 d以后, 土壤含水量均在40%以下, 在胁迫20 d时, 土壤含水量仅为 3.93%。复水后, 各个胁迫梯度的土壤含水量均有不同程度的增加, 且干旱5 d的土壤含水量恢复到了对照水平。
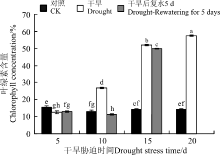
植株通过光合速率的调节来适应干旱环境, 而叶绿素含量与光合速率有着极大的相关性[25]。黄连花叶绿素含量在正常条件下呈现先降后增的趋势, 5 d时叶绿素含量最高, 为15.5%。干旱胁迫条件下, 黄连花叶绿素含量呈显著增加趋势(P< 0.05), 短期干旱胁迫下(5 d)为12.53%, 随着胁迫时间的延长开始大幅度上升, 并显著高于对照(P< 0.05), 在胁迫20 d时达到最大值(图5)。这可能是叶片含水量降低导致叶绿素含量相对升高引起的[26]。复水5 d后, 胁迫5 d的叶绿素含量稍有恢复, 但仍显著低于对照(P< 0.05)。胁迫10和15 d的叶绿素含量复水5 d后较胁迫条件下均有不同程度的下降, 其中干旱10 d的叶绿素含量的变化幅度较大, 而15 d的变化较小。
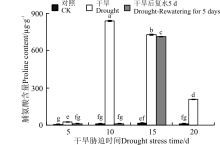
在逆境(干旱、盐碱)胁迫下, 植物体内会积累大量的脯氨酸, 其积累量与其本身的抗性有关[27]。随着干旱胁迫的加剧, 黄连花幼苗的脯氨酸含量呈现先上升后下降的趋势, 短期干旱(5 d)后, 脯氨酸含量与对照相比显著增加(P< 0.05), 但变化相对比较平缓。干旱胁迫10 d时急剧增加, 且达到最大值, 为839.25 μ g· g-1, 与对照相比, 增加了84.97倍。复水后, 胁迫5和10 d的脯氨酸含量显著减小, 与对照差异不显著(P> 0.05)。干旱15 d后复水5 d, 脯氨酸含量低于复水前, 但变化相对平缓(图6)。
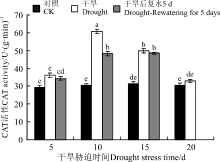
抗氧化酶(SOD、POD、CAT)活性对于干旱胁迫的响应不同, 三者协同发挥作用。5 d的干旱胁迫后, SOD活性变化不显著(P> 0.05)(图7), POD和CAT活性显著增加(P< 0.05)(图8、图9)。10 d的干旱胁迫后, 只有SOD活性显著下降, 而POD和CAT活性 依旧持续增加, 保持较高的活力, 且CAT活性达到了最大值。15和20 d的干旱胁迫后, CAT活性显著下降, 而POD活性依旧持续增加, 且在20 d时达到最大值。恢复供水后, 干旱5 d的POD活性较胁迫条件下显著增加, CAT依旧保持较高的活性, 说明短时间的干旱胁迫复水后, 植株清除活性氧的能力提升。干旱10 d复水后, SOD活性较胁迫条件下有所增加, POD和CAT活性下降。干旱15 d复水后, 三者的活性较胁迫条件下均变化不显著。
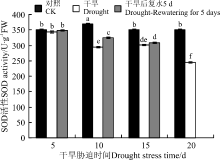 | 图7 干旱胁迫及复水后黄连花SOD活性Fig.7 The SOD activity of Lysimachia davurica after drought stress and rewatering |
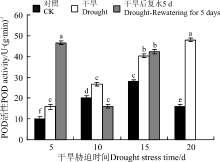 | 图8 干旱胁迫及复水后黄连花POD活性Fig.8 The POD activity of Lysimachia davurica after drought stress and rewatering |
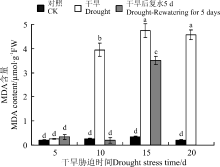
植物在逆境条件下, 会发生脂膜的过氧化, 产生丙二醛, 其浓度是判断脂质过氧化程度和膜系统伤害大小的指标[28]。随着胁迫时间的延长, 黄连花叶片中MDA含量呈现先增加后降低的趋势, 且在胁迫15 d时达到最大值(图10)。5 d的干旱胁迫对叶片中MDA含量的影响与对照相比差异不显著(P> 0.05), 10、15和20 d时叶片中MDA含量大量积累, 较对照 显著增加(P< 0.05), 说明此时的胁迫对细胞膜造成了一定程度的伤害。干旱10和15 d后复水5 d时, 叶片的MDA含量较胁迫条件下均有不同程度的下降, 特别是干旱10 d植株下部恢复生长的叶片MDA含量显著下降(P< 0.05), 且恢复到对照水平。说明经过10 d胁迫的黄连花幼苗复水后恢复能力很强, 经过短期的干旱胁迫膜系统可以迅速地恢复正常。而经过15 d胁迫的黄连花幼苗由于受到了严重的伤害, 短期内无法得到有效恢复。
可溶性糖是重要的渗透调节物质, 在遇到不良环境时, 可以启动防御机制[29]。对于黄连花, 随着胁迫时间的延长, 可溶性糖含量总体呈现为先增后降的趋势, 在10 d达到最大值(图11)。干旱5 d时, 植株受到的影响较小, 可溶性糖含量与对照相比变化不显著(P> 0.05)。10 d时, 开始大幅度上升, 与对照相比增加了24.45倍。随着时间的延长, 可溶性糖含量开始下降, 且在10~15 d时降幅较大。恢复供水后, 胁迫10 d的可溶性糖含量急剧下降, 且恢复到对照水平。胁迫15 d复水后, 可溶性糖含量有所下降, 与胁迫20 d时无显著差异。由此可见, 可溶性糖对于黄连花外界环境的变化较敏感, 在遭遇干旱胁迫时, 其在胁迫初期起着重要作用。
胁迫复水之后的成活率是衡量植株抗旱临界值的一个最简单直接的指标。通过对复水后黄连花成活率调查, 胁迫5和10 d复水之后成活率均为100%, 胁迫15 d复水之后, 成活率为66.67%, 而胁迫20 d的成活率为0。
干旱胁迫能显著抑制植株的生长发育, 且胁迫程度越高, 抑制作用就越大。本研究通过持续的干旱胁迫对影响植株正常生长发育的各指标进行了分析研究, 发现在胁迫时间低于10 d, 土壤含水量高于14.52%时, 黄连花的地上部分生长变慢, 此时及时地复水, 植株能恢复正常生长。当胁迫时间持续增加到15 d, 叶片严重失水, 地上部分干枯, 此时复水, 66.66%的植株可以重新长出幼苗。但当胁迫时间达到20 d时, 植株因缺水干旱死亡。说明黄连花地上部分可以承受10 d的干旱胁迫, 而整个植株的致死时间在15~20 d, 黄连花叶片死亡的胁迫程度并不代表整个植株的致死干旱胁迫程度。
叶绿素是光能吸收的主要物质, 直接影响植物光合作用的光能利用[30]。植物种类不同, 叶绿素对于干旱的响应也不同。干旱胁迫条件下, 紫穗槐(Amorpha fruticosa)、柽柳(Tamarix chinensis)、小叶锦鸡儿(Caragana microphylla)的叶绿素含量呈现先增加后下降的趋势[31], 而紫萼玉簪(Hosta ventricosa)的叶绿素含量不断降低[32]。本研究中, 随着胁迫程度的加深, 黄连花叶片叶绿素含量虽然出现了小幅度的波动, 但总体呈上升趋势。这与西北沼委陵菜(Comarum salesovianum)、树锦鸡儿(Caragana arborescens)等6种青藏高原植物在干旱胁迫下叶绿素呈现先降后升再降的趋势相似[26], 而茶菊(Chrysanthemum)的叶绿素含量随着胁迫程度的增加逐渐增加[33]。干旱胁迫下叶绿素含量变化的这种差异可能与植物自身的生物学特性和干旱胁迫发生的强度或持续时间有关, 至于干旱胁迫下叶绿素含量增加可能是叶片相对含水量降低, 每克叶干重、细胞数增加, 导致叶绿素浓缩[26], 含量上升。该现象可能是幼苗在干旱胁迫下维持光合速率的生理适应机制[23]。
干旱胁迫下, 植物代谢会发生紊乱, 细胞内会产生大量活性氧, 造成膜系统的损伤, 严重时会导致植物细胞死亡。植物自身为避免受活性氧的危害, 将主动调节抗氧化性酶类活性(SOD、POD和CAT)来清除体内的活性氧。但当活性氧产生太多, 超出了抗氧化保护系统的能力时, 会对膜系统造成伤害。SOD是清除细胞中多余O2-的重要保护酶, POD和CAT是清除H2O2的重要保护酶, 有研究表明, 在干旱胁迫下, 抗氧化物酶类活性一般会升高, 与抗旱性呈正相关[34, 35]。也有研究表明, POD在胁迫初期表现为清除作用, 表现为保护效应, 但是在逆境后期表达参与活性氧的生成, 叶绿素的降解, 并能引发膜脂过氧化作用, 表现为伤害效应[36]。本研究中, 胁迫5 d时土壤含水量显著下降, 而MDA含量与对照相比却无显著差异, 胁迫10 d时, MDA含量显著增加, 说明此时干旱胁迫对细胞膜造成了一定程度的伤害。随着胁迫时间的延长, 抗氧化保护酶系的POD活性大幅度增加, SOD活性下降, CAT活性在胁迫10 d时达到最大值, 随后下降。说明干旱胁迫下, 黄连花幼苗提高了其抗氧化保护酶活性, 从而保护细胞免受伤害。胁迫中CAT活性达到最大值后开始下降, 这可能是由于CAT的抵抗修复能力是有一定阈值的[37], 当胁迫超过10 d后, 将失去保护作用, 这与胁迫10 d复水后, MDA含量可恢复正常, 而胁迫15 d后无法恢复相符合。胁迫中SOD活性显著下降, 这可能与三者之间协同发挥作用[37], 从而减少活性氧的伤害有关。随着干旱胁迫时间的延长, 脯氨酸和可溶性糖含量均先增后减, 胁迫10 d时显著增加, 达到最大值, 说明二者在胁迫前期起重要作用, 而在胁迫后期, 可能是由于植株受到了严重伤害, 导致合成小于分解, 无法再调节植株的代谢。对于干旱10 d的黄连花幼苗进行复水, MDA、可溶性糖和脯氨酸含量均显著减少, 且恢复到对照水平, 说明黄连花的渗透调节能力和旱后恢复能力很强, 膜系统在复水后能迅速恢复, 保证其正常生长代谢。干旱5 d的黄连花复水后, POD活性显著提高, 而CAT活性保持较高的活性, 说明经过短期的干旱胁迫并复水后, 抗氧化保护酶活性维持在较高水平, 清除活性氧的能力提高。
通过以上分析, 本研究认为黄连花幼苗可以承受10 d的干旱胁迫, 主要是与较高的渗透调节能力和较强抗氧化能力以及复水后叶片的吸水能力和膜系统迅速恢复有关。短期的干旱胁迫(5 d)复水后, 植株的生长状况和对照无明显差别。因此, 黄连花在管理养护时, 可以进行短期的干旱胁迫, 在持续时间超过10 d时, 土壤含水量低于14.52%时, 应及时复水救苗。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|
| [34] |
|
| [35] |
|
| [36] |
|
| [37] |
|